Adrian Macion
Zakład Genetyki Bakterii
Instytut Mikrobiologii
SKN Biologii Molekularnej
Uniwersytet Warszawski
Ten adres pocztowy jest chroniony przed spamowaniem. Aby go zobaczyć, konieczne jest włączenie w przeglądarce obsługi JavaScript.
W 2020 roku została opracowana i wprowadzona do powszechnego użytku pierwsza szczepionka przeciwko SARS–CoV-2 firm Pfizer-BioNTech, powszechnie znana pod nazwą Comirnaty (BNT162b2). Głównym składnikiem szczepionki jest syntetyczne mRNA, które po wprowadzeniu do komórek ulega translacji i pozwala na ekspresję białka kolca wirusa. Powstałe białko jest wykrywane przez system odpornościowy organizmu, a wytworzona na drodze aktywacji immunologicznej odpowiedź i pamięć skutecznie chroni przed możliwą infekcją wirusową w przyszłości (układ odpornościowy, który już raz miał kontakt z antygenem, wytwarza komórki pamięci pozwalające na szybszą reakcję w przypadku powtórnego kontaktu; mechanizm ten nie prowadzi do uniemożliwienia infekcji, ale znacząco skraca jej czas trwania i zmniejsza powikłania).
Poniższa grafika przedstawia fragment dokumentu wydanego przez WHO (ang. World Health Organisation – Światowa Organizacja Zdrowia), który opisuje biochemiczną strukturę materiału podawanego w preparacie.
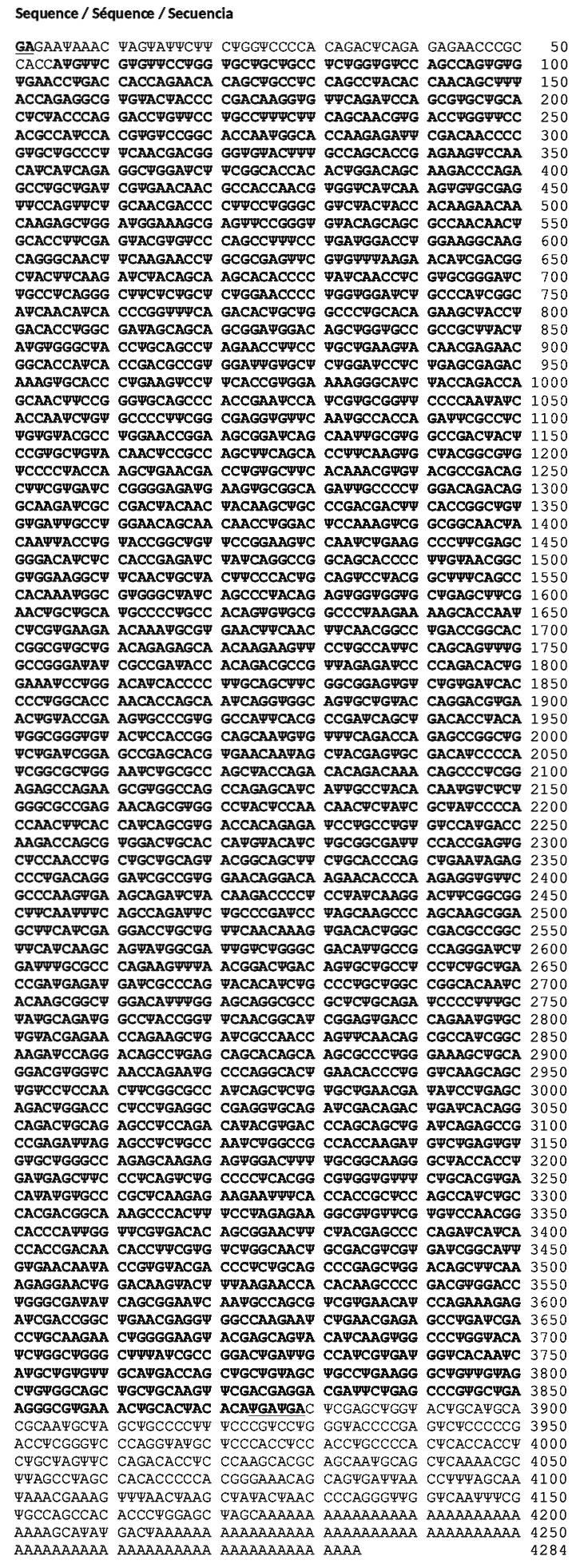
Pełna długość sekwencji RNA podawanego w szczepionce wynosi 4284 nukleotydy. Nie jest ona jednak wierną kopią mRNA kodowanego przez genom wirusa, na którego ma uodparniać. Sekwencja zawiera odpowiednie modyfikacje, które nie tylko zwiększają intensywność translacji, ale także chronią RNA przed częścią mechanizmów degradujących kwasy nukleinowe obcego pochodzenia, których głównym zadaniem jest zabezpieczanie komórek przed infekcja wirusową
Struktura sekwencji szczepionkowej rozpoczyna się od elementu znanego jako cap, który odpowiada za stabilizację cząsteczki RNA od końca 5’ i umożliwia rozpoznanie jej przez mechanizmy translacyjne komórki. Dzięki regionowi cap mRNA ze szczepionki lokalizuje się na rybosomach, które bezpośrednio odpowiadają za syntezę białek.
Region 5’-UTR (ang. untranslated region; region niepodlegający translacji) przedstawia sekwencja:
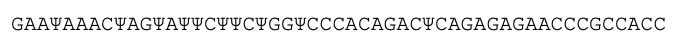
Na typ etapie widoczna już jest jedna z podstawowych modyfikacji mRNA szczepionkowego – podczas gdy w klasycznych cząsteczkach mRNA występują cztery zasady azotowe – A, U, G i C – w mRNA szczepionkowym zasada U została zastąpiona Ψ (1-metylo-3′-pseudourydyna). Modyfikacja ta ma za zadanie chronić mRNA przed degradacją przy użyciu nukleaz komórkowych, które stanowią zabezpieczenie antywirusowe. W trakcie translacji Ψ rozpoznawane jest jednak jako normalne U – zamiana ta więc nie zaburza procesu syntezy białka.
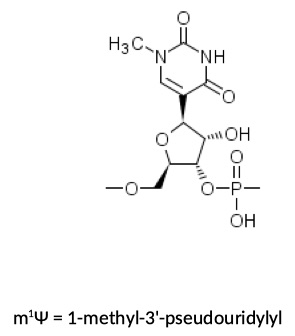
Pozostała część 5’-UTR jest dostosowana w celu optymalizacji syntezy białka. Dzięki niesieniu odpowiednich danych pozwala na kontrolę inicjacji i postępu translacji – a poprzez to – ostatecznie na syntezę białka w optymalnej ilości.
Kolejny odcinek szczepionkowego mRNA koduje peptyd sygnałowy – region białka, który odpowiada za jego odpowiednią lokalizację w komórce. Region ten jednak również ulega modyfikacji (w porównaniu do natywnej sekwencji wirusowej). Górny odcinek przedstawia fragment mRNA wirusowego, a dolny – fragment mRNA szczepionkowego:
W zaznaczonych rejonach widoczne są różnice polegające za zamianie pojedynczych nukleotydów (należy pamiętać, że Ψ odczytywane jest jako U – dlatego modyfikacje te nie są tu zaznaczone). Jaki jest cel takiej modyfikacji? Zmiany w ostatnich nukleotydach trójek kodujących (kodonów) zazwyczaj nie zmieniają kodowanego przez tę trójkę aminokwasu. W zamieszczeni poniżej tabeli kodu genetycznego widać, że większość aminokwasów jest kodowanych przez różne kodony (w genetyce zjawisko to nazywane jest degeneracją kodu genetycznego):
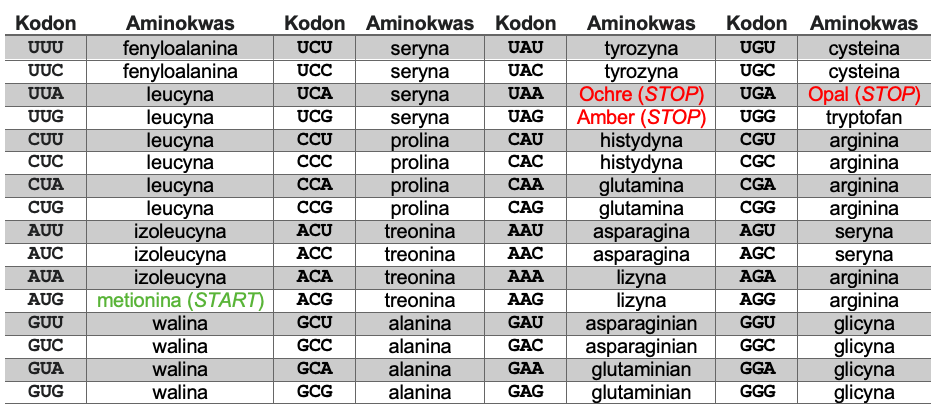
Wprowadzone w sekwencji peptydu sygnałowego modyfikacje pozwalają więc na syntezę niezmienionego białka, jednak okazuje się, że mRNA zawierające więcej reszt C i G znacznie lepiej podlega translacji niż jego uboższa w te sekwencje wersja.
Po sekwencji kodującej peptyd sygnałowy lokalizuje się odcinek kodujący właściwe białko S o długości 3777 nukleotydów. Sekwencja ta również podlega modyfikacjom (podobnymi jak całą reszta mRNA szczepionkowego): (I) zastąpienie U przez stabilizujące mRNA Ψ; (II) optymalizacja zwiększająca zawartość C i G. To jednak nie wszystko. Sekwencja kodująca białko S zawiera dodatkową zmianę, która jest niezbędna do właściwego działania szczepionki:
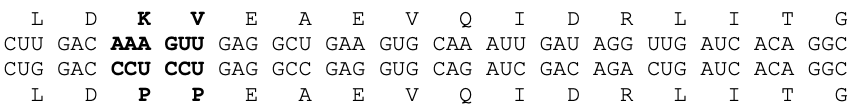
Aminokwasy numer 2 i 3 zostały zmienione (2: K –> P; 3: V –> P). Takie modyfikacje sekwencji aminokwasowej pozwalają na produkcję białka, które przyjmie właściwą strukturę przestrzenną i będzie przez układ odpornościowy wykrywane w podobny sposób jak białko pochodzące bezpośrednio od wirusa lub komórki zainfekowanej.
Zmodyfikowany jest również koniec 3’ genu, którego kodon STOP (oznaczający miejsce zakończenia syntezy białka, a w sekwencji poniżej oznaczony literą s) jest podwojony. Zwiększa to skuteczność terminacji translacji i zapobiega syntezie białka o wydłużonej domenie C-terminalnej.

Niekodująca białko sekwencja ulokowana na końcu 3’ przyjmuje najbardziej zoptymalizowaną postać, która odpowiada nie tylko za zwiększenie wydajności syntezy białka, ale także stabilności cząsteczki mRNA.
Jak widzimy w powyższym tekście – zaplanowanie konstrukcji czegoś tak prostego, jak licząca zaledwie 4284 nukleotydy cząsteczka mRNA nie jest wcale takie proste, jednak ta niedługa sekwencja na zawsze zmieniła naszą rzeczywistość i sposób walki z chorobami zakaźnymi.