Dominika Kalinowska
IX LO im. Klementyny Hoffmanowej w Warszawie
Wrodzona odpowiedź immunologiczna pozwala na błyskawiczne rozpoznanie i unieszkodliwienie patogenów tudzież nieprawidłowych komórek. Komórki NK (Natural Killer) wywołują śmierć komórek nowotworowych lub zakażonych wirusami. W poniższej pracy przedstawione są dwa najważniejsze mechanizmy wykrywania nieprawidłowych komórek, dzięki którym NK mogą indukować ich apoptozę.
NK to duże ziarniste limfocyty różnicujące się z protoplastów limfoidalnych (z których różnicują się także limfocyty T i B) dzięki czynnikom transkrypcyjnym T-box (T-bet i EOMES). Dojrzewają w szpiku kostnym, węzłach chłonnych, śledzionie, grasicy i migdałkach. Stanowią one 5–10% limfocytów krążących we krwi obwodowej. Pełnią istotną funkcję w mechanizmie wrodzonej odpowiedzi immunologicznej. Niszczą komórki zainfekowane wirusami i zmienione nowotworowo bez konieczności wytworzenia przeciw nim odporności swoistej. NK nie potrzebują zewnętrznej aktywacji do unieszkodliwiania komórek, którym brak antygenów MHC I (stąd nazywane są naturalnymi zabójcami). Są zdolne do produkcji IFN-γ (interferonu gamma) i TNF-α (czynnika martwicy nowotworów, ang. tumor necrosis factor) Wykazują dwa zasadnicze mechanizmy wykrywania komórek, które należy unieszkodliwić.
Pierwszym z mechanizmów jest wykrywanie zmniejszonej liczby molekuł MHC I (bądź zupełnego ich braku) na powierzchni danych komórek. NK posiadają specjalne receptory dla MHC I, które są jednocześnie inhibitorami ich działania. Wszystkie prawidłowe komórki organizmu wykazują ekspresję antygenów MHC I. Obecność odpowiedniej liczby tych cząsteczek na powierzchni komórki hamuje indukowanie apoptozy przez NK. Synteza MHC I jest znacząco zmniejszona u komórek nowotworowych. Komórki NK wykrywają to, dzięki czemu mogą je unieszkodliwić. Komórki zakażone wirusami zwiększają ekspresję tzw. ligandów aktywujących, czyli dla których NK posiadają receptory. Pobudzenie tych receptorów stymuluje działanie NK. To, czy NK uruchomią mechanizm odporności przeciw danej komórce, zależy od stosunku pobudzonych receptorów na powierzchni NK. Jeżeli przeważa sygnał receptorów aktywujących, NK rozpoczną kaskadę reakcji doprowadzających do śmierci danej komórki. Jeżeli przeważa sygnał receptorów dla MHC I, nie dojdzie do indukcji apoptozy u rozpoznawanej komórki. Ryc. 1. przedstawia trzy sytuacje, w których komórka NK rozpoznaje antygeny występujące na powierzchni pewnej komórki ciała. Dwie spośród sytuacji prowadzą do degranulacji NK i indukcji apoptozy komórki.
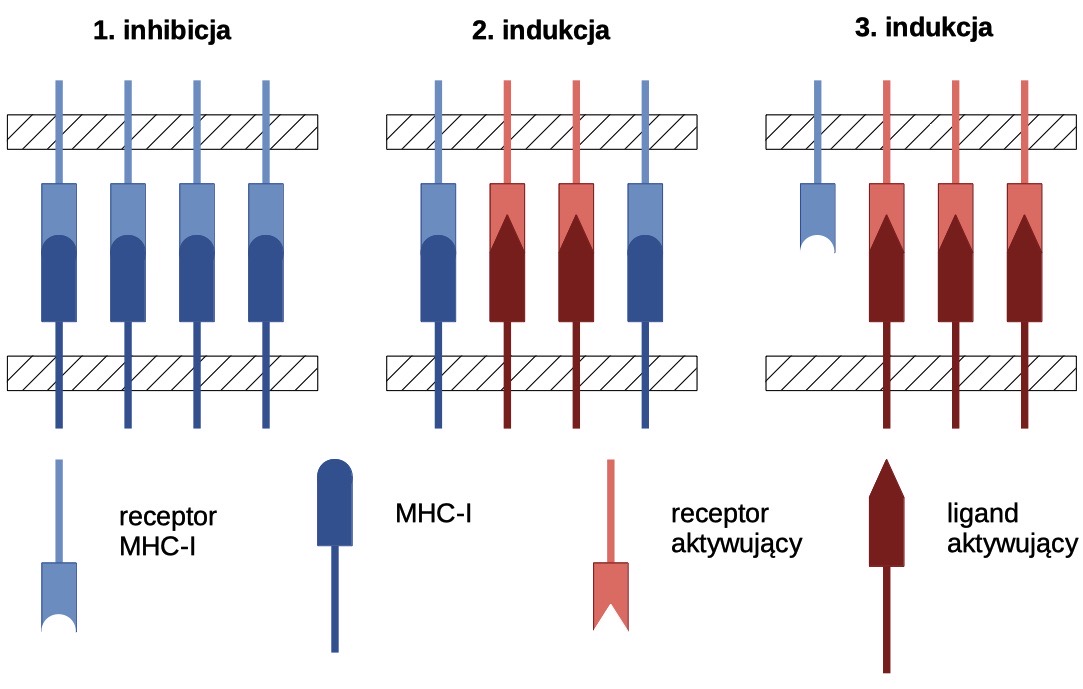
Ryc. 1. Aktywacja komórek NK.
W drugim mechanizmie działania komórki NK wykorzystują fakt, że komórki zakażone wirusami i nowotworowe wytwarzają antygeny, przeciw którym została już wytworzona odporność swoista i przyczepiły się do nich IgG. NK posiadają na swojej powierzchni receptory CD16, które po połączeniu się z regionem Fc IgG aktywują mechanizm cytotoksyczności komórkowej zależnej od przeciwciał (ADCC, ang. Antigen Dependent Cell Cytotoxicity). Opisany wyżej mechanizm został ukazany na Ryc. 2.
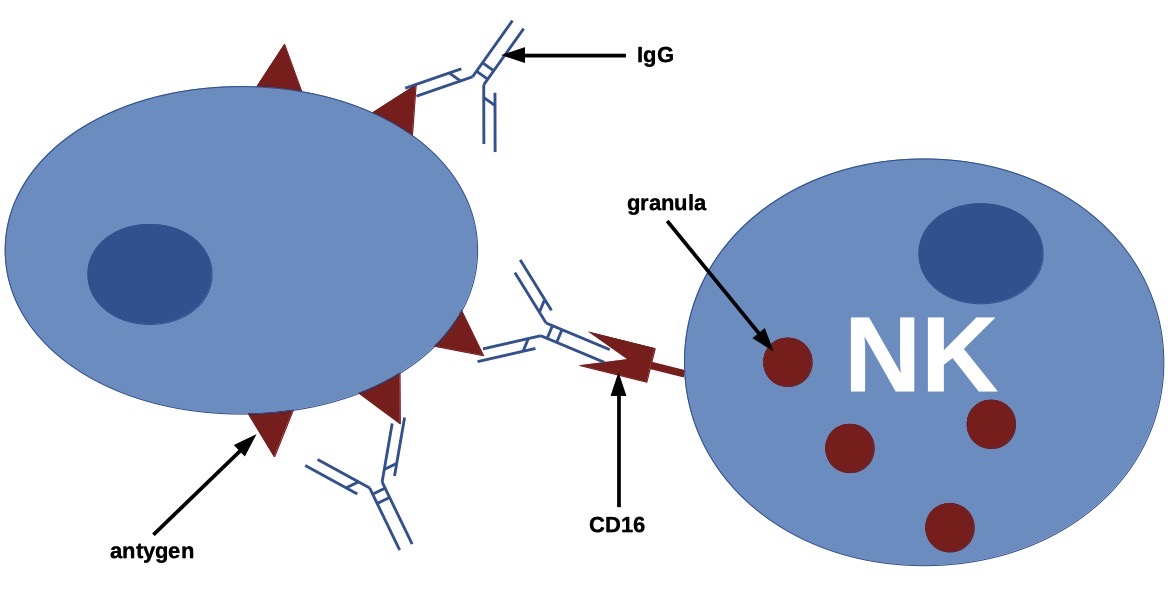
Ryc. 2. Mechanizm ADCC (cytotoksyczności zależnej od przeciwciał) u NK.
Pobudzenie komórki NK indukuje jej degranulację. Masowej egzocytozie ulegają pęcherzyki (granule), w których znajdują się białka: perforyny i granzymy. Perforyny wraz z białkami układu dopełniacza tworzą domenę MACPF (Membrane Attack Complex/Perforin). Penetrują docelową błonę komórkową i oligomeryzują (dzięki zmianie stężenia Ca²⁺) w kanały dla granzymów. Granzymy to proteazy serynowe, które po wniknięciu do komórki rozpoczynają kaskadę aktywacji kolejnych kaspaz. Kaspazy (ang. caspases – cysteine aspartic proteases) to proteazy, które pełnią kluczową funkcję w programowanej śmierci komórki. W komórce występują w formie zymogenu, w związku z czym wymagają aktywacji poprzez konkretne bodźce, aby wykonać swoją pracę. Wyróżnia się kaspazy inicjatorowe (2, 8, 9, 10) i efektorowe (3, 6, 7). Ryc. 3. przedstawia uproszczony schemat oddziaływań kolejnych kaspaz ze sobą. Kaskada rozpoczyna się od aktywacji kaspazy-8, która polega na połączeniu ze sobą dwóch prokaspaz-8 w heterotetramer (prokaspazy inicjatorowe posiadają małą i dużą podjednostkę). Następnie kaspaza-8 aktywuje kaspazę-3. Kaspaza-3 aktywuje kolejne czynniki proapoptotyczne, w tym DNazę aktywowaną kaspazami, która degraduje materiał genetyczny komórki. Granzym posiada też inną, znaczącą funkcję. Zmienia strukturę białka Bid, które oddziałuje z białkami Bax i Bak. Białka te tworzą pory w błonach mitochondrialnych, zwiększając ich przepuszczalność, a to skutkuje uwolnieniem cytochromu c. To umożliwia utworzenie apoptosomu. Powstaje on poprzez przyłączenie się cytochromu c do domeny WD-40 czynnika APAF1 (Apoptotic protease activating factor 1) oraz przyłączenie i aktywację prokaspazy-9 przed domenę CARD. Aktywna kaspaza-9 oddziałuje na kolejne kaspazy efektorowe, m.in. na wspomnianą wcześniej kaspazę-3. Kaskada kończy się apoptozą komórki, podczas której zachodzą również takie procesy jak tworzenie ciałek apoptotycznych i odwodnienie cytoplazmy. Można zauważyć, że dla powyższych procesów kluczowa jest m.in. inicjatorowa kaspaza-8. Ekspresja jej genu zachodzi konstytutywnie w warunkach fizjologicznych. Wyciszenie bądź usunięcie tego genu skojarzone są z nerwiakiem zarodkowym, nowotworem złośliwym neuroblastów.
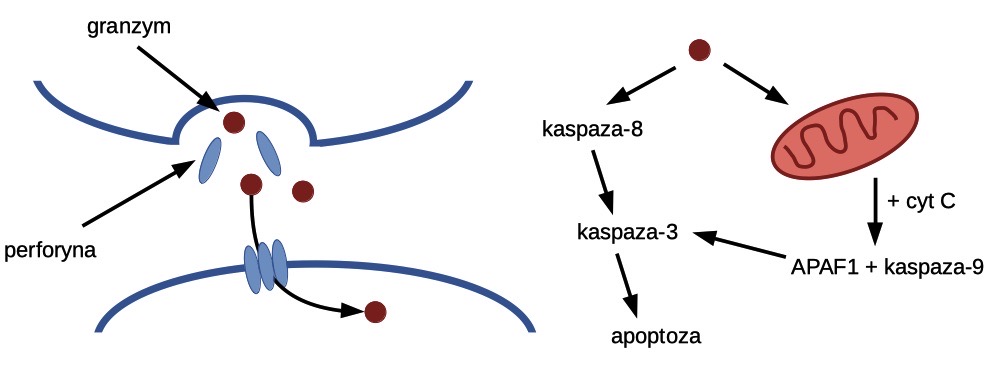
Ryc. 3. Uproszczony molekularny mechanizm apoptozy.
Warto dodać, że istnieje specjalny podtyp NK – uNK (uterine NK). Aby zarodek mógł się rozwinąć, układ odpornościowy kobiety w ciąży ulega supresji. uNK należą do podtypu CD54 (NCAM) NK, ulegają pobudzeniu w reakcji na cytokiny, lecz cechuje je niska cytotoksyczność. Stanowią 70% leukocytów in utero w trakcie ciąży. Komórki trofoblastu hamują syntezę HLA-A i HLA-B w celu uniknięcia wytworzenia odporności przez limfocyty T, co normalnie pobudziłoby do działania NK, a dzięki temu nie ma miejsca. Trofoblast selektywnie akumuluje HLA-E i HLA-G, które są inhibitorami działania uNK, więc chronią zarodek przed indukowaną przez te komórki apoptozą.
Źródła:
- Kuby, Janis. Kuby Immunology. New York: W.H. Freeman, 2013
- Berg, L. R., Martin, C., Martin, D. W., & Solomon, E. P. Biology, 2014
- Ainhoa Arina, Oihana Murillo, Juan Dubrot, Arantza Azpilikueta, Carlos Alfaro, Jose L Pérez-Gracia, Maurizio Bendandi, Belen Palencia, Sandra Hervás-Stubbs & Ignacio Melero (2007) Cellular liaisons of natural killer lymphocytes in immunology and immunotherapy of cancer, Expert Opinion on Biological Therapy, 7:5, 599-615
- Cerwenka, A., Lanier, L. Natural killer cells, viruses and cancer. Nat Rev Immunol 1, 41–49 (2001)
- Abel Alex M., Yang Chao, Thakar Monica S., Malarkannan Subramaniam. Natural Killer Cells: Development, Maturation, and Clinical Utilization. Front. Immunol., 13 August 2018
- Chen, M., Wang, J. Initiator caspases in apoptosis signaling pathways. Apoptosis 7, 313–319 (2002)